手机 App 已上线
点我下载
有人看到这个题目,马上就会不置可否的说,才半年有效那还打什么疫苗!
希望有这种想法的网友能够耐心看看文章。
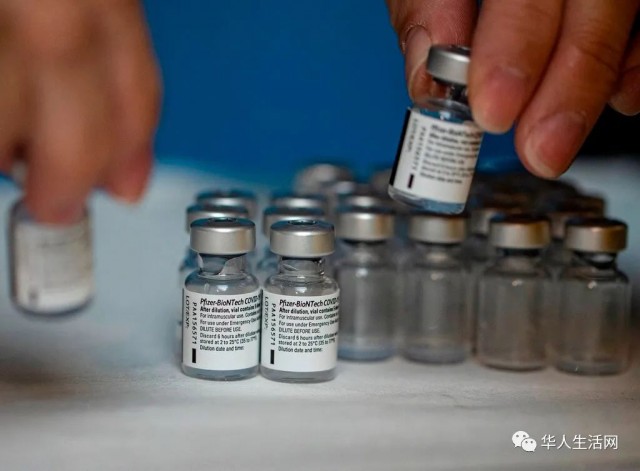
根据最新消息,辉瑞/BioNTech周四表示,其新冠疫苗的保护作用在第二剂疫苗接种后能至少持续6个月。
6个月虽然不算长,但是这不是一个固定的数字,在几个月前,疫苗厂商宣布的有效期是3个月,因为这个数字是根据厂商自己的三期试验得出来的结果。
目前,三期试验后续有效性的试验还正在进行中,也就是说凡是在试验中接种了安慰剂和疫苗组的民众依旧在不断的被随访,更新数据,迄今为止,该数据更新到了6个月。
如果再过几个月,疫苗在这些三期试验者身上继续有效,那么厂商会继续更新疫苗的有效期。
我们在这里,也再次感谢这些伟大的志愿者!同时也感谢疫苗厂商,用详实的数据来说话,为防疫工作做出科学保证。
3月31日,辉瑞/BioNTech两家公司说,在六个月内,数据显示这种疫苗的有效性仍在91%以上,而对令人担忧的B.1.351变种完全有效,当然这一数据还没有大量的数据作为基础,只在南非招募了800名志愿者,而美国还没有大范围B.1.351传播,所以科学家表示谨慎继续关注。
辉瑞和BioNTech在一份联合声明中表示:“该疫苗对疾病控制和预防中心(CDC)定义的重症100%有效,对食品和药物管理局(FDA)定义的重症有效率为95.3%。”
据悉,FDA对重症的定义包括表明
呼吸窘迫的呼吸频率升高;
心律加快,血氧饱和度低于93%;
严重的呼吸衰竭,需要额外吸氧或换气;
表明休克的血压下降;
严重的肾、肝或神经功能障碍,进入重症监护病房或死亡
而CDC对重症的定义包括血氧饱和度等于或低于94%,X线检查发现肺部浸润(肺炎的一种指征)大于50%。
辉瑞公司董事长兼首席执行官博拉(Albert Bourla)在声明中表示:“这些数据证实了我们的疫苗有良好的功效和安全性,并使我们能够向FDA提交生物制剂许可申请(BLA)。”BLA是完全批准的申请,辉瑞疫苗目前已获得紧急使用授权(EUA),但尚未获得全面批准。
博拉还表示:“在第二剂接种后长达6个月的时间里,(我们)都观察到疫苗的高度有效,并可抵御B.1.351变种,这进一步增强了对我们疫苗整体有效性的信心。
超过4.6万名志愿者参加了辉瑞疫苗试验,在他们中发现了927例出现症状的新冠病例,其中850人属于安慰剂组,剩下77人属于疫苗组。
所有患者中观察到32例CDC定义的重症病例,全部在安慰剂组。而根据FDA对重症的定义,在安慰剂组观察到21例病例,疫苗组观察到1例。
该公司在B.1.351变种流行的南非招募了800名志愿者参与试验,其中观察到9例新冠病例,均在安慰剂组,表明疫苗对B.1.351变种100%有效。
